前列腺癌(prostate cancer, PCa)多数初诊患者已近晚期,雄激素阻断治疗(androgen deprivation treatment, ADT)是较公认的措施。但经1.5~2.0年ADT敏感期,几乎所有患者均转为“去势不敏感”状态,即“去势抵抗性前列腺癌(castration-resistant prostate cancer, CRPC)”。
本文研究的是 神经内分泌前列腺癌(Neuroendocrine prostate cancer,NEPC),属于 CRPC的一种,最恶性,而且罕见。
然后本研究很多分析都引用了 Neuroendocrine Prostate Cancer (Trento/Cornell/Broad 2016)数据集,http://www.cbioportal.org/study?id=nepc_wcm_2016#summary 如果要理解本文,同时需要了解 该数据集的 81个病人的114个测序样本。发表于 Nat Med. 2016 , 该文章同时还有 关于 prostate adenocarcinomas (CRPC-Adeno) and neuroendocrine prostate cancer (CRPC-NE) 的区别的探索,转录组数据。奇怪的是该数据集本身就很复杂,还包括meta分析,Integrated NEPC score analysis across 604 samples from four different RNA-Seq prostate cancer datasets。
为什么类器官优于 人源肿瘤异体移植模型(PDX) ?
前列腺癌背景
全球范围内前列腺癌(Prostate Cancer)的发病率在男性所有恶性肿瘤中位居第二。在美国,前列腺癌的发病率已超过肺癌而成为第一位危害男性健康的肿瘤。据统计,当今男性终生患前列腺癌的风险为16%,对于50岁以上的男性,患病率高达42%。
搜索关键词:【前列腺癌的 激素 治疗 抵抗】 可以查到下面这些资讯。
前列腺癌的治疗方法包括手术、放射治疗及内分泌治疗。
内分泌治疗通过阻断雄激素促使雄激素依赖性癌细胞凋亡,从而达到治疗目的。对于晚期或进展期前列腺癌,内分泌治疗是主要的治疗手段,绝大多数患者对内分泌治疗敏感。 前列腺癌的内分泌治疗已有75年的历史。前列腺癌的内分泌治疗开创了恶性实体肿瘤内分泌治疗的先河;内分泌治疗是前列腺癌的主要治疗方法。由于对前列腺癌内分泌治疗的卓越研究成果,Huggins、Schally分别获得1966年、1977年诺贝尔生理学和医学奖。
激素敏感型前列腺癌内分泌治疗方法主要包括:
- ①去势治疗:手术去除产生睾酮的器官或抑制产生睾酮器官的功能,包括手术或药物去势(包括GnRHa和雌激素);
- ② 抗雄激素药物治疗:应用抗雄激素药物竞争性阻断雄激素与前列腺癌细胞上雄激素受体的结合;
- ③最大限度雄激素阻断疗法:去势治疗联合抗雄药物治疗。
但经14-30个月的内分泌治疗后,大多数患者逐渐进展为去势抵抗前列腺癌(CRPC),并且多数患者伴有骨转移或远处脏器的转移。这些转移性CRPC患者预后差,预计生存期 <19个月。以多西他赛(Docetaxel)为基础的化疗已成为目前临床上公认的治疗CRPC的有效方案。但,对于多西他赛治疗失败的CRPC目前仍是医学上的难题。
自2010年以来,到2016年,已有包括 Provenge、Jevtana、Zytiga、Xtandi和Xofigo在内的5款可用于治疗CRPC的新药获美国FDA批准上市。这些药物的问世不仅为CPRC的治疗提供了新的治疗手段,同时还有望激活抗前列腺癌药物市场。随时前列腺癌的逐渐上升,新型CRPC治疗药物有望成为行业研发热点。
神经内分泌前列腺癌(Neuroendocrine prostate cancer,NEPC)是一种致命的疾病,总体生存期一般不超过1年。NEPC大多数情况下是对转移性去势抵抗性前列腺癌(mCRPC)应用雄激素剥夺治疗(Androgen deprivation therapy,ADT)治疗的“后遗症”。
现有把这个NEPC一般当做是小细胞肺癌来治疗,但是预后很差: - small cell neuroendocrine prostate cancer 的 NCI-H660 细胞系
- castration-resistant neuroendocrine prostate cancer (CRPC-NE)
所以作者希望构建CRPC-NE的类器官类器官等模型的构建
流程图如下:
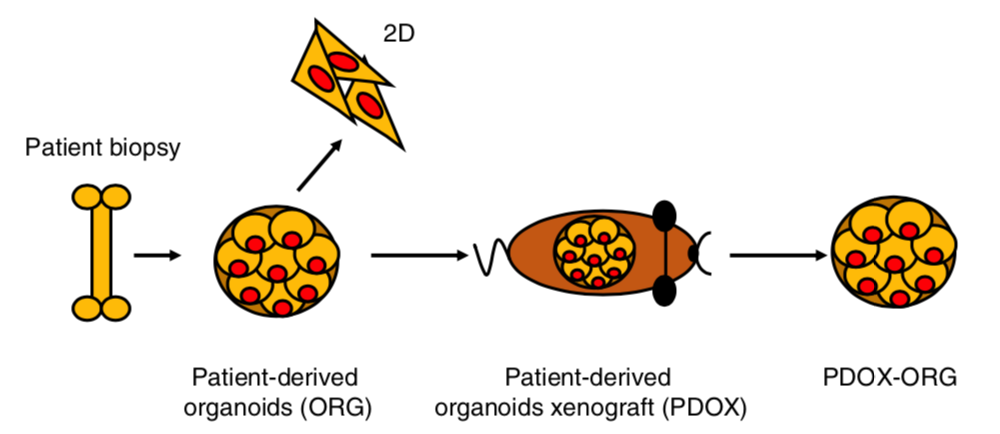
首先是从病人体内拿到 needle biopsies. - In the scheme a patient biopsy is processed to generate 3D organoids (ORG).
- 3D organoids are then used to generate 2D cultures (2D) and also engrafted in an NSG mouse to grow patient-derived organoids xenograft (PDOX) and consequent organoids derived from the PDX (PDOX-ORG)
总体上来说,是围绕着类器官这个科研热点,构建成功了这个癌症研究模型!表达量探索
主要是利用了前面提到的发表于 Nat Med. 2016 文章的数据来跟自己构建的类器官等模型表达情况相比较, 包括:
- published cohort of 26 localized prostate adenocarcinoma PCA
- 33 metastatic castration-resistant adenocarcinoma (CRPC-Adeno)
- 13 CRPC-NE patient samples
- CRPC-NE organoids (orange)
- CRPC-NE PDOX (green)
- NIC-H660 cell line (red)
首推PCA分析的可视化结果咯:
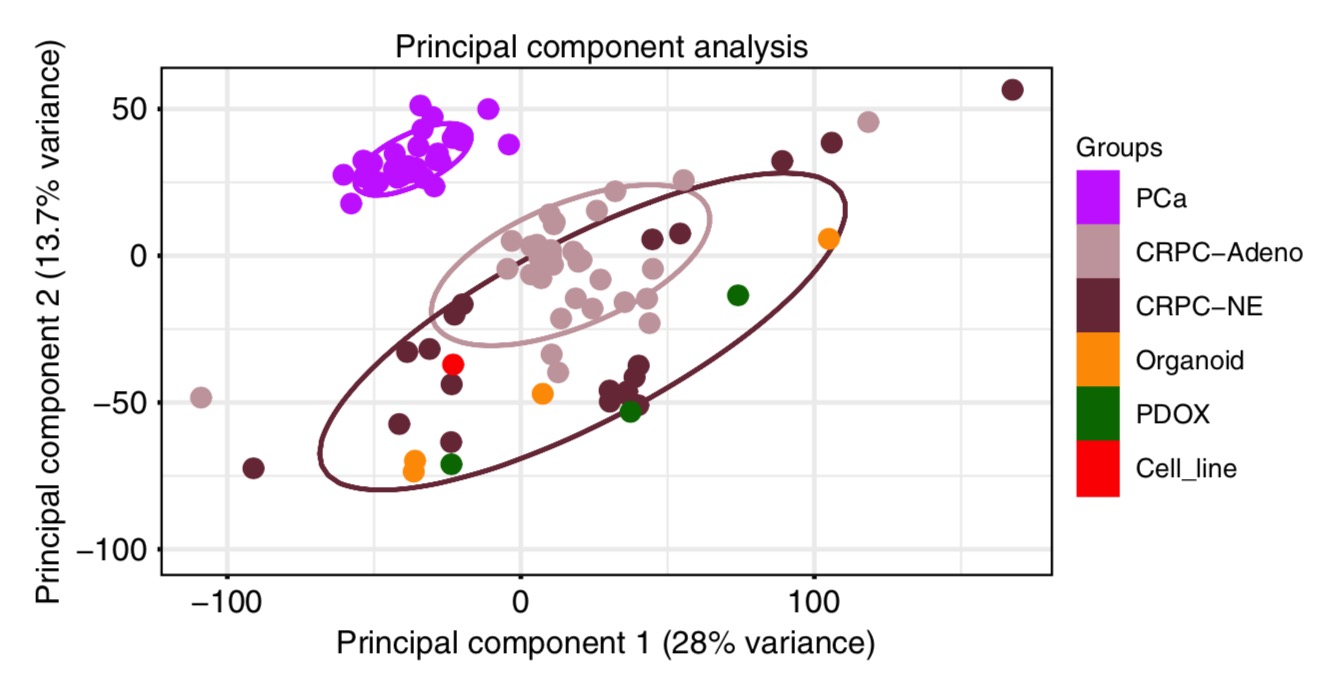
然后是一个非常标准的热图,这个热图选取的也是发表于 Nat Med. 2016 文章得到 CRPC-NE signature genes 列表:
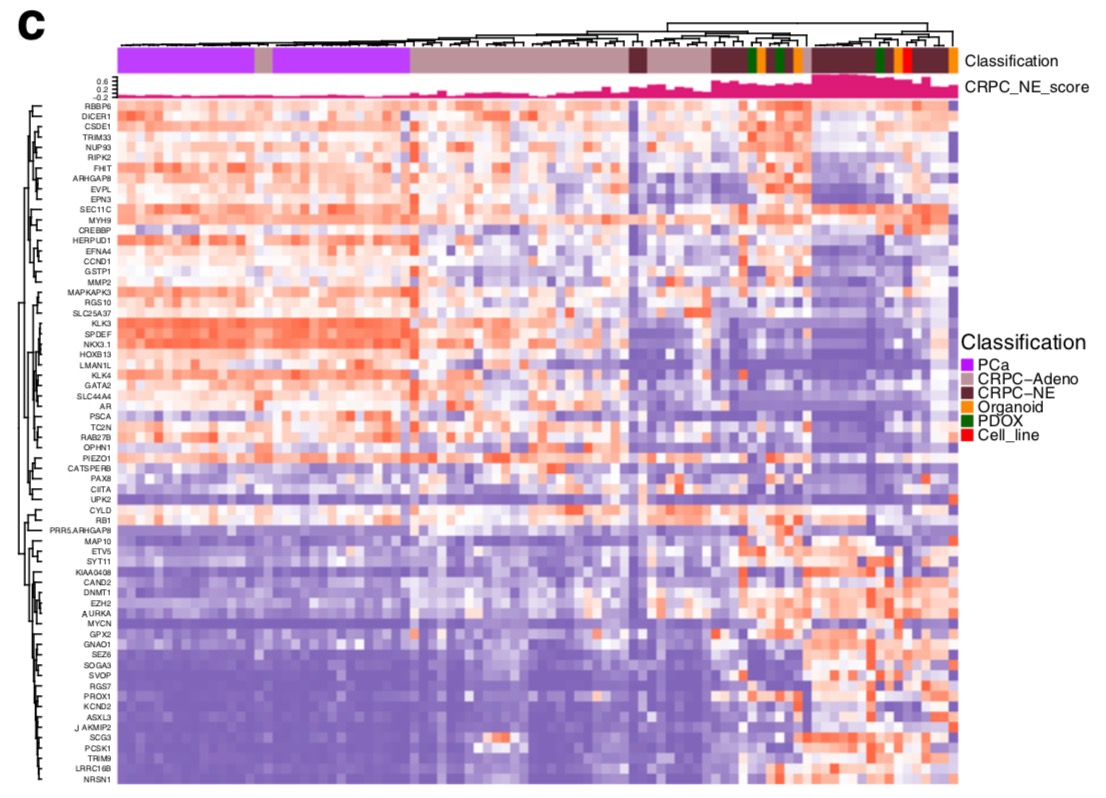
表观数据结果
主要是 enhanced reduced representation bisulfite sequencing (ERRBS) 数据,最后也是看相关性:
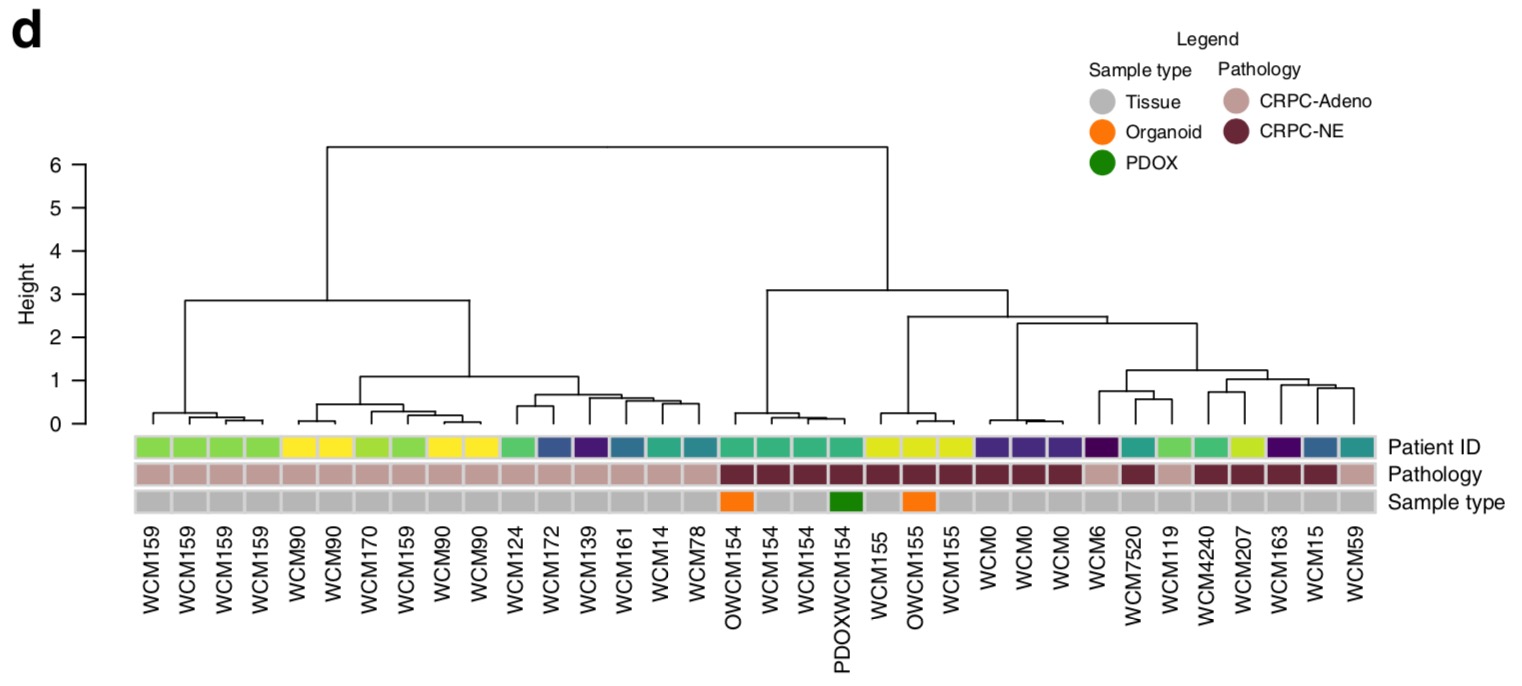
变异情况探索
这里只涉及到成功培养了类器官的那4个病人,包括他们的各种状态的样本,但是能下载的只有下面13个数据:
| ID | label | description |
| —————————————————————————————— | ———————- | —————————————————————————————- |
| SRR6957179 | PDOXWCM1262 | subcute tumor explant from organoids of pelvic mass |
| SRR6957178 | OWCM1262 | organoids from pelvic mass |
| SRR6957177 | PDOXWCM154 | subcute tumor explant from organoids of bone biopsy |
| SRR6957176 | PDOX-ORGWCM1078 | subcute tumor explant from organoids of lymph node biopsy2 |
| SRR6957175 | PDOXWCM1078 | subcute tumor explant from organoids of lymph node biopsy1 |
| SRR6957174 | 2DWCM155 | 2D organoids fromliver biopsy |
| SRR6957173 | OWCM155_2 | organoids fromliver biopsy2 |
| SRR6957172 | OWCM1078_2 | organoids from lymph node biopsy2 |
| SRR6957171 | OWCM1078_1 | organoids from lymph node biopsy1 |
| SRR6957170 | OWCM154_2 | organoids from bone biopsy_2 |
| SRR6957169 | OWCM154_1 | organoids from bone biopsy_1 |
| SRR6957168 | OWCM155_1 | organoids fromliver biopsy1 |
| SRR6957167 | 2DWCM154 | 2D organoids from bone biopsy |
可能是由于隐私的问题,作者把病人自身的测序数据给上传到了dbGAP比较难以下载,事实上作者的结论是这些培养物比较好的保留了肿瘤病人的肿瘤部位的特征,你们这些数据的公开其实和公开肿瘤病人自身的数据没有太大的区别。
既然是肿瘤外显子数据,就走标准分析流程,得到可靠的somatic变异信息,以及拷贝数变异情况。
首先看跟CRPC-NE癌症相关的基因的拷贝数变化,在同一个病人的不同培养物都显示出一致的变化,如下;
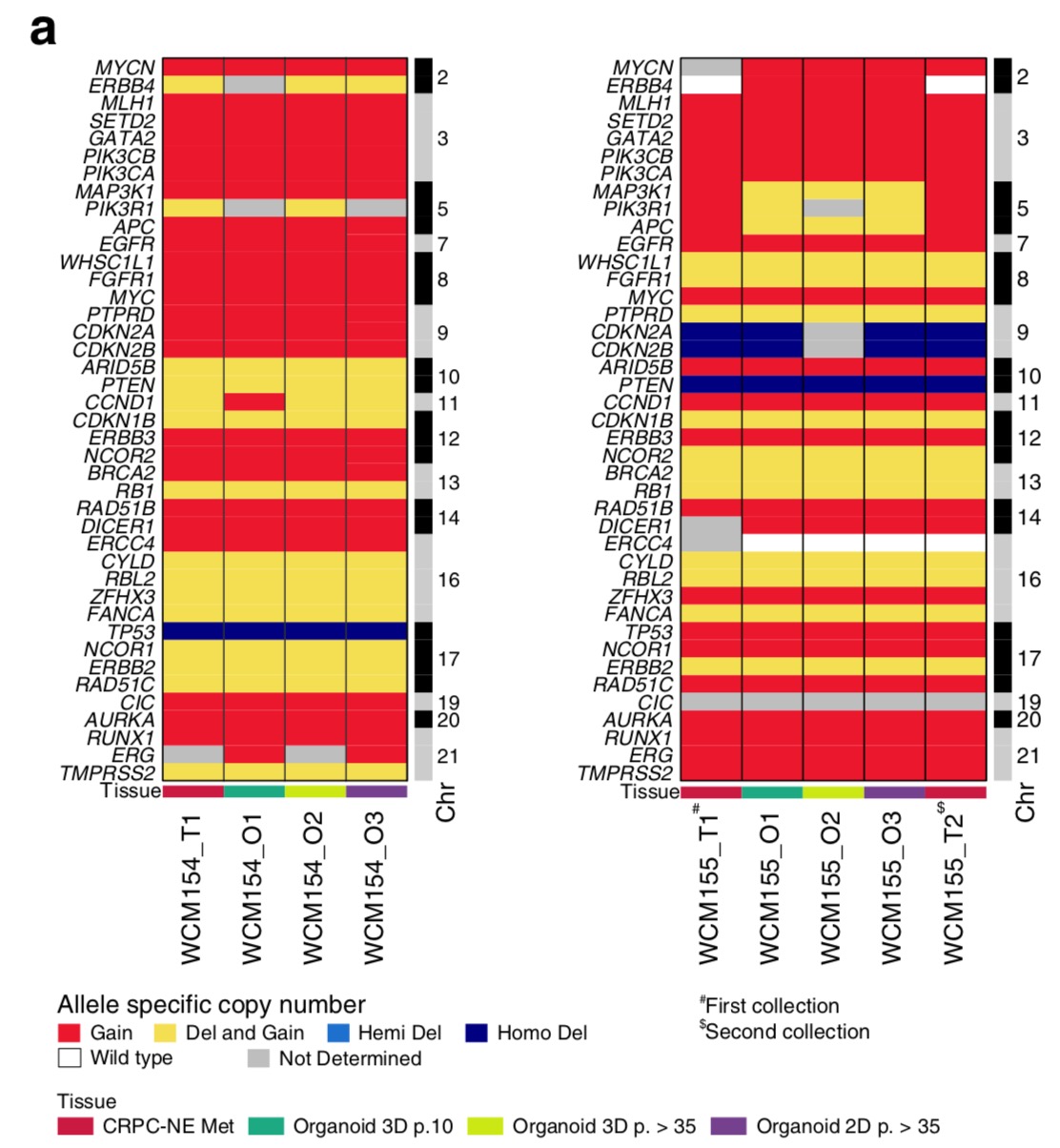
当然了,从基因组全局所有染色体范围看,也是这个一致性:
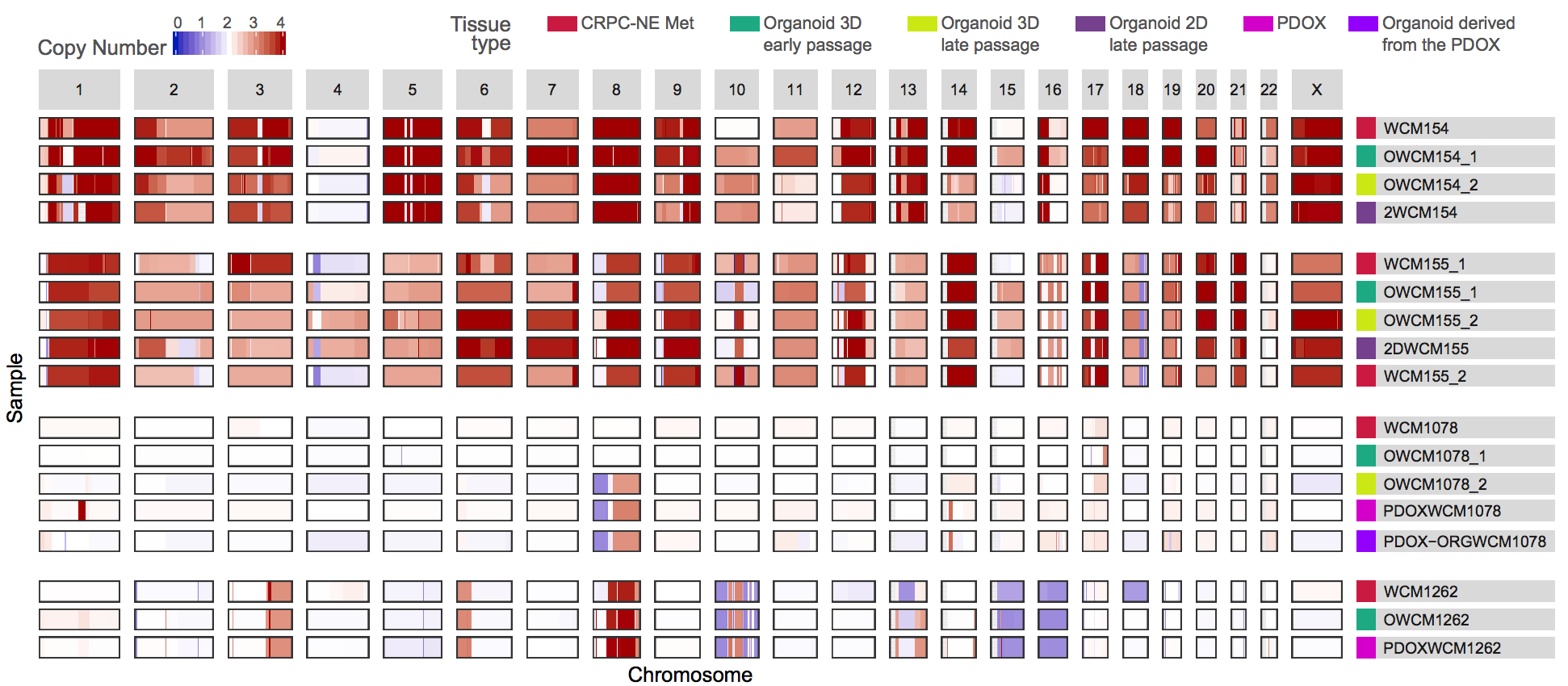
值得注意的是这里作者使用的是CLONET软件来计算肿瘤纯度和肿瘤的倍性:
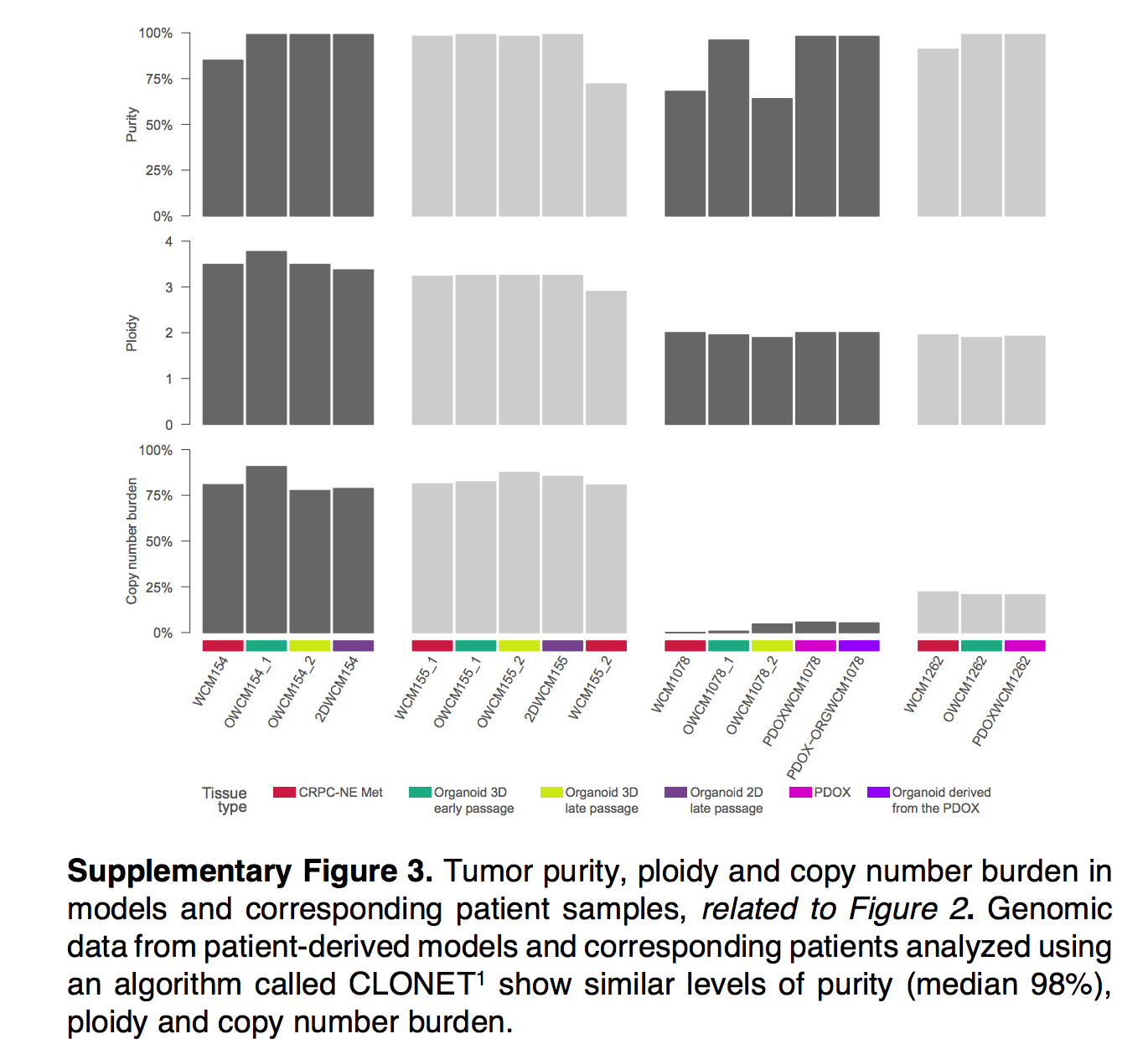
可以看到肿瘤纯度很多都解决与 100% , 而且肿瘤的倍性也很一致。
因为这个软件我没有用过,可能要个把月之后才能回过头来看看是怎么回事。
结论:模型能完美模拟其对应的CRPC-NE病人
包括:
- consistent IHC analysis of common markers
- genomic alterations
- mRNA and DNA methylation clustering
这些数据分析结果都得到同样的结论高通量药物筛选
这个偏实验,就暂不解读!
数据公开
作者自己的数据分成4部分
- 转录组数据:GSE112830
- 外显子数据: SRP138000.
- ERRBS数据:GSE112830
- 还有部分人类隐私数据:dbGap:phs000909.v.p1 (http://www.cbioportal.org/study?id=nepc_wcm_2016)